Fluoreto de césio
Sobre este escolas selecção Wikipedia
Esta seleção é feita para as escolas de caridade infantil leia mais . SOS Children trabalha em 45 países africanos; você pode ajudar uma criança em África ?
| Fluoreto de césio | |
|---|---|
 | |
 | |
Fluoreto de césio | |
Outros nomes Fluoreto de césio | |
| Identificadores | |
| Número CAS | 13400-13-0 |
| ChemSpider | 24179 |
| Número RTECS | FK9650000 |
| Imagens-jmol 3D | Imagem 1 |
SMILES
| |
InChI
| |
| Propriedades | |
| Fórmula molecular | CsF |
| Massa molar | 151,90 g / mol |
| Aparência | sólido cristalino branco |
| Densidade | 4,115 g / cm 3 |
| Ponto de fusão | 682 ° C (955 K) |
| Ponto de ebulição | 1251 ° C (1.524 K) |
| Solubilidade em água | 367 g / 100 ml (18 ° C) |
| Estrutura | |
| A estrutura de cristal | cúbico, CF8 |
| Grupo espacial | Fm 3 m, No. 225 |
| Coordenação geometria | Octaédrico |
| Momento de dipolo | 7.9 D |
| Perigos | |
| MSDS | MSDS External |
| Índice da UE | Não listado |
| Ponto de centelha | Não inflamável |
| Os compostos relacionados | |
| Outros aniões | Cloreto de césio Brometo de césio Iodeto de césio |
| Outros cátions | Fluoreto de lítio O fluoreto de sódio Fluoreto de potássio Fluoreto de rubídio |
Excepto quando indicado, os dados são dados para materiais no seu estado normal (a 25 ° C, 100 kPa) | |
| Referências de Infobox | |
Fluoreto de césio (fluoreto de césio na América do Norte), é um composto inorgânico normalmente encontrado como um sólido branco higroscópico. Ela é mais solúvel e mais facilmente dissociado do que fluoreto de sódio ou fluoreto de potássio. Encontra-se disponível na forma anidra, e se a água tenha sido absorvida é fácil de secar por aquecimento a 100 ° C durante duas horas in vácuo. Como todos os fluoretos solúveis, é ligeiramente de base. Um facto interessante sobre este composto é que é o composto mais iónico. O césio tem o menor electronegatividade (excepto frâncio, um elemento radioactivo extremamente rara instável), e o flúor tem a maior electronegatividade.
Síntese e propriedades
Fluoreto de césio é preparada pela acção de ácido fluorídrico em ou hidróxido de césio carbonato de césio, seguido de remoção de água.
Fluoreto de césio reage geralmente como uma fonte de ião fluoreto, F -. É, portanto, é submetido a todas as reacções usuais associados com fluoretos solúveis, por exemplo:
- 2 CsF + CaCl2 → 2 CsCl + CaF2
A estrutura de cristal
Fluoreto de césio tem a estrutura halito, o que significa que o Cs + e F - um pacote em cúbica matriz compactada mais próximo como fazem Na + e Cl - em cloreto de sódio. Catiões de césio são maiores do que aniões fluoreto, enquanto que nos halogenetos de lítio, sódio, potássio, e de rubídio, os catiões são menores do que o anião.
Aplicações
Na síntese orgânica
Sendo altamente dissociados é uma fonte mais reativo de fluoreto de sais relacionados. CSF é menos higroscópico alternativa para fluoreto de tetra-n-butilamónio (TBAF) e TAS-flúor (TASF) quando anidro "naked" fluoreto de ião é necessária.
Como uma base de
Tal como acontece com outros fluoretos solúveis, CsF é moderadamente básica, porque HF é um ácido fraco. A baixa nucleofilicidade de flúor significa que pode ser uma base útil em fluoreto chemistry.Caesium orgânico é uma base útil em química orgânica , devido ao facto de o fluoreto de iões é um relativamente pobre nucleófilo. CsF dá rendimentos mais elevados em Reacções de condensação de Knoevenagel que KF ou NaF.
Formação de ligações CF
Fluoreto de césio também é uma fonte popular de flúor na química organofluorine. Por exemplo, reage com CsF hexafluoroacetona para formar um sal de césio perfluoroalkoxide, que é estável até 60 ° C, ao contrário do correspondente de sódio ou de potássio de sal. Ele irá converter deficientes em electrões cloretos de arilo para fluoretos de arilo ( reacção halex).
Agente de desprotecção
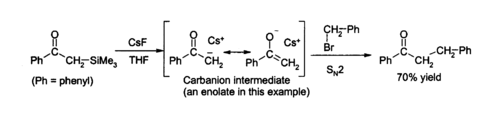
Devido à resistência do Si - F ligação, de iões de fluoreto é útil para reações desililação (remoção de grupos Si) em química orgânica ; fluoreto de césio é uma excelente fonte de fluoreto anidro para tais reacções. A remoção dos grupos de silício ( dessilila�o) é uma grande aplicação para a PSC no laboratório, como o próprio natureza anidro permite a formação limpa de água intermediários sensíveis ao. Soluções de fluoreto de césio em THF ou DMF atacar uma vasta variedade de compostos de organo-silício para produzir um fluoreto de organo-silício e um carbanião, o qual pode então reagir com eletrófilos, por exemplo:
A dessililação é também útil para a remoção de silil grupos protectores.
Outros usos
Um único cristal de sal são transparentes para o abismo infravermelho. Por esta razão, é por vezes usado como as janelas de células utilizadas para espectroscopia de infravermelho.
Precauções
Como outros fluoretos solúveis, CsF é moderadamente tóxico. Contato com ácido devem ser evitados, como esta formas altamente tóxico / corrosivo ácido fluorídrico. Césio ião (Cs +), ou de cloreto de césio, não é geralmente considerado tóxico.