Tolueno
Sobre este escolas selecção Wikipedia
Arranjar uma seleção Wikipedia para as escolas no mundo em desenvolvimento sem internet foi uma iniciativa da SOS Children. Para comparar instituições de caridade de patrocínio esta é a melhor ligação de patrocínio .
| Tolueno | |
|---|---|
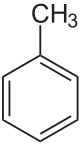 | 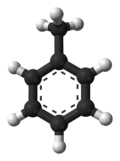 |
Metilbenzeno | |
Outros nomes tolueno | |
| Identificadores | |
| Número CAS | 108-88-3 |
| PubChem | 1140 |
| ChemSpider | 1108 |
| UNII | 3FPU23BG52 |
| DrugBank | DB01900 |
| KEGG | C01455 |
| Chebi | Chebi: 17578 |
| ChEMBL | CHEMBL9113 |
| Número RTECS | XS5250000 |
| Imagens-jmol 3D | Imagem 1 |
SMILES
| |
InChI
| |
| Propriedades | |
| Fórmula molecular | C 7 H 8 |
| Massa molar | 92.14 g mol-1 |
| Aparência | Líquido incolor |
| Densidade | 0,87 g / ml (20 ° C) |
| Ponto de fusão | -95 ° C, K 178, -139 ° F () |
| Ponto de ebulição | 111 ° C, 384 K, 232 ° F () |
| Solubilidade em água | 0,47 g / L |
| Índice de refracção (n D) | 1.497 (20 ° C) |
| Viscosidade | 0,590 cP (20 ° C) |
| Estrutura | |
| Momento de dipolo | 0.36 D |
| Perigos | |
| MSDS | MSDS External |
| Frases R | R11, R38, R48 / 20, R63, R65, R67 |
| Frases-S | (S2), S36 / 37, S29, S46, S62 |
| Principal Perigos | altamente inflamável |
| NFPA 704 |  3 2
0 |
| Ponto de centelha | 6 ° C (43 ° F) |
| Valor Limite | 50 mL de m-3, 190 mg de m -3 |
| Os compostos relacionados | |
| Relacionado hidrocarbonetos aromáticos | benzeno xileno naftalina |
| Os compostos relacionados | metilciclohexano |
| Página Suplementar dados | |
| Estrutura e Propriedades | N, ε r, etc. |
| Termodinâmica dados | Comportamento de fase Sólido, líquido, gasoso |
| Os dados espectrais | UV, IV, RMN , MS |
Excepto quando indicado, os dados são dados para materiais no seu estado normal (a 25 ° C, 100 kPa) | |
| Referências de Infobox | |
Tolueno, anteriormente conhecido como toluol, é uma clara, água líquida -insoluble com o cheiro típico de tíner. É um mono-substituído benzeno derivado, isto é, uma em que um único átomo de hidrogénio de um grupo de seis átomos da molécula de benzeno foi substituído por um grupo univalente, neste caso CH3.
É um hidrocarboneto aromático que é amplamente usado como um industrial matéria-prima e como um solvente . Como outros solventes, de tolueno é também, por vezes, utilizadas como uma drogas inalantes por suas propriedades intoxicantes; no entanto, a inalação de tolueno tem potencial para causar danos neurológicos graves. O tolueno é um solvente orgânico importante, mas também é capaz de dissolver um número de produtos químicos inorgânicos notáveis, tais como enxofre, iodo, bromo, fósforo. e outras substâncias não-covalentes polares.
História
O composto foi isolado pela primeira vez em 1837 por um Químico polonês Filip Walter através de uma destilação de pinho óleo que deu o nome retinaptha. Este nome foi substituído pouco depois por tolueno por uma palavra derivada do nome toluol mais velho, que se refere a tolu bálsamo, um extrato aromático da árvore tropical colombiana Balsamum Myroxylon, a partir da qual também foi isolado depois. Ele foi originalmente chamado por Jöns Jakob Berzelius.
Propriedades químicas
Adicionou-se tolueno reage como um normais hidrocarboneto aromático direcção substituição aromática electrofílica. O grupo metilo torna cerca de 25 vezes mais reactivo do que o benzeno em tais reacções. Ela sofre suave sulfonação para dar ácido p-toluenossulfónico, e cloração por Cl 2 , na presença de FeCl3 para dar orto e para isómeros de clorotolueno. Ela sofre nitração para dar orto e para isômeros nitrotolueno, mas se aquecido pode dar dinitrotolueno e, finalmente, o explosivo trinitrotolueno (TNT).
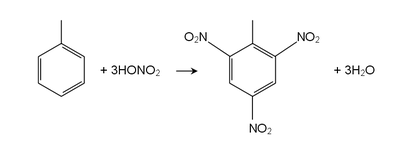
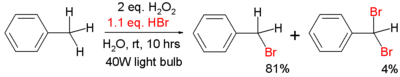
Com outro Reagentes de metilo cadeia lateral em tolueno pode reagir, submetidos a oxidação. A reacção com permanganato de potássio e ácido diluído (por exemplo, ácido sulfúrico ) ou permanganato de potássio com concentração de ácido sulfúrico , conduz à ácido benzóico, enquanto que a reacção com cloreto de cromilo leva a benzaldeído ( Reacção Etard). A halogenação pode ser realizada sob condições de radicais livres. Por exemplo, N-bromo-succinimida (NBS) aquecido com tolueno, na presença de AIBN leva a brometo de benzilo. Adicionou-se tolueno também pode ser tratado com elementar bromo , na presença de luz UV (luz solar directa) para se obter brometo de benzilo. Tolueno podem também ser bromado por tratamento com HBr e H 2 O 2 na presença de luz.
Catalisador de hidrogenação de tolueno para metilciclohexano requer uma alta pressão de hidrogénio para ficar completa, devido à estabilidade do sistema aromático. pKa é de aproximadamente 45.
Produção
Tolueno ocorre naturalmente em níveis baixos no petróleo bruto e é geralmente produzido nos processos de tomada através de uma gasolina reformer catalítico, numa etileno biscoito ou fazer coque de carvão . A separação final, quer através de destilação ou extracção com solvente, tem lugar em um dos muitos processos disponíveis para a extracção da Aromáticos BTX (benzeno, tolueno e xileno) isómeros.
Preparação
Tolueno podem ser preparados industrialmente ou no laboratório por uma variedade de métodos.
- A partir de benzeno ( Reacção Friedel-Crafts)
O benzeno reage com o cloreto de metilo em presença de cloreto de alumínio anidro para formar tolueno. A formação segue um mecanismo de reacção de substituição electrof:
- CH3 Cl + AlCl3 → CH3 + + AlCl 4 -
- C 6 H 5 CH 3 H + + + AlCl 4 - → C 6 H 5 CH 3 + HCl + AICI3
Os seguintes catalisadores podem ser usados em lugar de AlCl3:
- AlCl3> SbCl 3> SnCl4> BF 3> ZnCl2> HgCl2
Note-se que a reacção não é muito útil como o derivado de mono-alquilo formado sofre rapidamente mais de alquilação a uma velocidade ainda maior, para produzir produtos polissubstituídos.
- A partir de bromobenzeno ( Reação Wurtz-Fittig)
A reacção Wurtz-Fittig é a reacção de um halogeneto de arilo e um halogeneto de alquilo na presença de metal de sódio para dar origem a compostos aromáticos substituídos.
Quando bromobenzeno e brometo de metilo reagir com o metal de sódio em solução de éter seco, obtém-se tolueno.
- C 6 H 5 Br + CH 3 Br + 2Na → C 6 H 5 CH 3 + 2NaBr
- A partir de ácido toluico ( decarboxylation)
Quando o sal de sódio do ácido toluico ( o-, m-, p) é aquecida com cal de soda, obtém-se tolueno.
- C 6 H 4 CH 3 COONa (toluato de sódio) + NaOH → C 6 H 5 CH 3 (tolueno) + Na 2 CO 3
- A partir de cresol
Quando cresol (o-, m-, p-) é destilado com pó de zinco, obtém-se tolueno.
- C 6 H 4 CH 3 OH (cresol) + Zn → C 6 H 5 CH 3 (tolueno) + ZnO
- A partir de ácido toluenossulfónico
Quando o ácido toluenossulfónico é tratado com vapor sobreaquecido ou cozido com HCI, obtém-se tolueno.
- CH 3 C 6 H 4 SO 3 H (ácido toluenossulfónico) + HOH (vapor) → C 6 H 5 CH 3 (tolueno) + H 2 SO 4 ( ácido sulfúrico )
- A partir de toluidine
Toluidina é diazotado com primeiro de nitrito de sódio (NaNO 2) e HCl a baixa temperatura. O composto de diazónio assim obtida é aquecida com alcalina cloreto estanoso (SnCl2). Esta reacção dá tolueno.
- A partir de Reagente de Grignard
Quando brometo de fenil magnésio (C 6 H 5) MgBr é feito reagir com brometo de metilo, obtém-se tolueno.
Usos
O tolueno é um comum solvente , capaz de dissolver tintas, diluentes de tintas, selantes de silicone, muitos reagentes químicos , borracha , tintas de impressão, adesivos (colas), lacas, curtidores de couro, e desinfetantes. Ele também pode ser usado como um Indicador de fulereno, e é uma matéria-prima para di-isocianato de tolueno (utilizados no fabrico de espuma de poliuretano) e TNT. Além disso, ele é utilizado como um solvente para criar uma solução de nanotubos de carbono. É também usado como um cimento para fino poliestireno kits (por dissolução e, em seguida, fundindo as superfícies), uma vez que pode ser aplicada com muita precisão por escova e não contém nenhum dos grandes quantidades de um adesivo.
Utilizações industriais incluem desalquilação de tolueno a benzeno, e o desproporcionação a uma mistura de benzeno e xileno. Quando oxidada cede benzaldeído e ácido benzóico, dois intermediários importantes na química. É também usado como uma fonte de carbono para fazer multi-Parede Nanotubos de carbono. O tolueno pode ser utilizado para quebrar células vermelhas do sangue a fim de extrair hemoglobina em experimentos de bioquímica.
O tolueno pode ser usado como um impulsionador do octano em combustíveis de gasolina utilizada em motores de combustão interna. Tolueno a 86% em volume abastecido todos os turbo equipes de Fórmula 1 na década de 1980, foi pioneiro primeiro pela equipe Honda. Os restantes 14% foi um "enchimento" de n-heptano, para reduzir o índice de octanas para satisfazer Fórmula 1 restrições de combustível. Tolueno a 100% pode ser usado como combustível para motores de dois tempos e de quatro tempos; no entanto, devido à densidade do combustível e outros factores, o combustível não vaporizam facilmente, a menos que pré-aquecido a 70 graus Celsius (Honda realizada esta na sua carros de Fórmula 1 através do encaminhamento das linhas de combustível através do sistema silenciador para aquecer o combustível). Tolueno também coloca problemas semelhantes aos combustíveis álcool, como ele come através das linhas de combustível padrão de borracha e não tem propriedades lubrificantes, como a gasolina padrão faz, que pode quebrar as bombas de combustível e causar desgaste diâmetro do cilindro superior.
Na Austrália, o tolueno foi encontrado para ter sido combinado com gasolina ilegalmente em lojas de combustíveis para a venda como combustível veicular padrão. Tolueno atrai este imposto não combustível, enquanto outros combustíveis são tributados em mais de 40%, por isso os fornecedores de combustível são capazes de lucrar com a substituição do tolueno mais barato para a gasolina. Esta substituição é susceptível de afectar o desempenho do motor e resultar em desgaste adicional. O grau de substituição de tolueno não foi determinada.
O tolueno é um outro em um grupo de combustíveis que têm sido recentemente utilizadas como componentes de combustível de aviação misturas de aluguel. O tolueno é utilizado como um jet substituto de combustível para o seu teor de compostos aromáticos.
Tolueno também tem sido usado como um refrigerante para as suas boas capacidades de transferência de calor em armadilhas de sódio fria utilizadas em circuitos de sistema de reactor nuclear.
Tolueno também tinha sido utilizado no processo de removendo a cocaína de folhas de coca na produção de xarope de Coca-Cola.
Biologia
Semelhante a muitos outros solventes, tais como 1,1,1-tricloroetano e alguns alquilo benzenos , tolueno foi mostrado que actua como um não competitivo E antagonista do receptor de NMDA Receptor GABAA modulador alostérico positivo. Ele é abusado como uma inalantes provavelmente por conta da eufórico e efeitos dissociativos estas ações produzem. Além disso, o tolueno foi mostrado para exibir efeitos do tipo antidepressivo em roedores no teste de natação forçada (FST) e da teste de suspensão pela cauda (TST).
Toxicologia e metabolismo
Tolueno não deve ser inalado devido aos seus efeitos sobre a saúde. Os baixos níveis a moderada pode causar cansaço, confusão, fraqueza, ações do tipo de embriaguez, perda de memória, náuseas, perda de apetite, e ouvir e cor perda de visão. Estes sintomas geralmente desaparecem quando a exposição está parado. Inalar níveis altos de tolueno em um curto período de tempo pode causar tonturas, náusea, ou sonolência. Ela também pode causar perda de consciência, e até mesmo a morte.
O tolueno é, contudo, muito menos tóxico do que o benzeno , e tem, como consequência, em grande parte substituído-lo como um solvente aromático na preparação química. Por exemplo, o benzeno é um agente cancerígeno conhecido, enquanto tolueno tem muito pouco potencial carcinogénico.